As bactérias e o segredo para a cura da AIDS
A Síndrome da Imunodeficiência Adquirida (AIDS) é uma doença do sistema imunológico decorrente da infecção pelo Vírus da Imunodeficiência Humana (HIV).Apesar dos progressivos avanços da medicina farmacêutica no desenvolvimento de medicamentos antivirais, o vírus é capaz de se refugiar no interior das células por meio da união do DNA viral ao DNA humano, escapando da ação de tais medicamentos e das defesas naturais do organismo. As células contendo esses segmentos de DNA viral atuam como reservatórios de HIV e constituem o principal obstáculo para a cura definitiva da AIDS.
O tratamento atual consiste na utilização de medicamentos antivirais, compostos por substâncias que combatem o vírus na corrente sanguínea. Entretanto, a grande limitação desses tratamentos deve-se ao fato de o HIV, diferente de outros vírus como o da gripe, pertencer a um grupo chamado de retrovírus, os quais são capazes de utilizar a sua maquinaria celular para inserir seu DNA nas células do hospedeiro. Com isso, além de provocar a morte de algumas células, especialmente as do sistema imune, ele cria reservatórios de HIV no interior das mesmas e, ao se interromper o tratamento com medicamentos antivirais, a infecção é capaz de se reiniciar. Esses reservatórios podem se localizar em diferentes tecidos do corpo como os órgãos linfáticos, células intestinais e até no cérebro. Por esse motivo, tais reservatórios são os principais alvos para uma cura definitiva da AIDS e a edição genética é um dos principais campos de pesquisa a buscar mecanismos que atuem diretamente na eliminação dessas reservas.

Dadas as limitações apresentadas pelos tratamentos existentes, a tecnologia CRISPR/Cas9 surge como uma poderosa ferramenta de edição genética ao atuar diretamente nesses reservatórios, permitindo modificar regiões genômicas específicas por meio da remoção dos trechos de DNA viral.
Recentemente, um experimento realizado por cientistas do Lewis Katz Schoolof Medicine da Universidade de Temple, conseguiu remover completamente o vírus HIV (tipo HIV-1) de linfócitos T humanos isolados utilizando uma poderosa técnica de edição genética conhecida como CRISPR/Cas9. Tal técnica baseia-se no primitivo sistema imunológico bacteriano e foi descoberta pela bioquímica americana Jennifer Doudna e a microbiologista francesa Emmanuelle Charpentier em estudos com Escherichia coli. O mecanismo do CRISPR/Cas9 identifica o DNA invasor e armazena fragmentos dele no próprio DNA da bactéria, de tal forma a protegê-la de elementos genéticos externos como plastídios e vírus, assegurando que a bactéria e sua descendência possam se defender em futuras infecções.
O mecanismo de reconhecimento do DNA externo consiste no pareamento de sequências complementares situadas no DNA bacteriano e no invasor. Em um trecho do DNA circular bacteriano, situa-se uma pequena região - com cerca de 20 a 50 pares de bases - bastante característica, denominada locus CRISPR (do inglês Clustered Regularly Interspaced Short Palindromic Repeats). Essa região caracteriza-se pela presença de curtas repetições do DNA bacteriano, regularmente interespaçadas por fragmentos nucleotídicos denominados espaçadores. Esses espaçadores, porém, provém dos elementos externos que adentraram a bactéria, ou seja, são partes recortadas do material genético invasor que a bactéria armazena para si. Isso é a chamada memória imunológica bacteriana, dado que, uma vez introduzido um segmento de DNA invasor no DNA bacteriano, podem se passar anos, décadas, milênios, que a bactéria e sua descendência serão capazes de reconhecê-lo em um novo contato.
Ademais, adjacente à região dos espaçadores, o locus CRISPR possui sequências codificantes de proteínas denominadas Cas (do inglês CRISPR Associated Proteins), que são endonucleases altamente específicas, responsáveis por reconhecer e recortar o DNA invasor, ou seja, são as tesourinhas do genoma. Tomando de exemplo a infecção por um bacteriófago a uma Escherichia coli temos que: em uma primeira infecção (Figura 1A), a endonuclease Cas9 identifica a introdução de um DNA invasor, liga-se a ele e recorta um pequeno fragmento que então, com o auxílio das endonucleases Cas1 e Cas2, será levado ao locus CRISPR e introduzido como um novo espaçador, criando um registro permanente daquele invasor, ou seja, conferindo memória imune à bactéria.
Em uma segunda infecção (Figura 1B), a bactéria, ao reconhecer a entrada do DNA invasor, expressa o gene completo dessa região, criando uma longa cadeia de RNA que contém todas as sequências armazenadas no DNA bacteriano, sem distinção. Esse RNA, logo após ser expresso, é fragmentado exatamente entre as regiões espaçadoras de DNA invasor, originando segmentos de crRNAs (do inglês CRISPR RNA). Juntamente com a região CRISPR, são expressas também as proteínas pertencentes a essa região, especialmente a endonuclease Cas9. Cada um dos fragmentos do crRNA é então inserido em uma Cas9, deixando-a altamente específica, de tal forma que, ao reconhecer o DNA do invasor que se pareia com o RNA dentro da enzima, a Cas9 é capaz de cliva-lo. Com isso, a bactéria se torna capaz de reconhecer todos os DNAs que um dia já a invadiram.
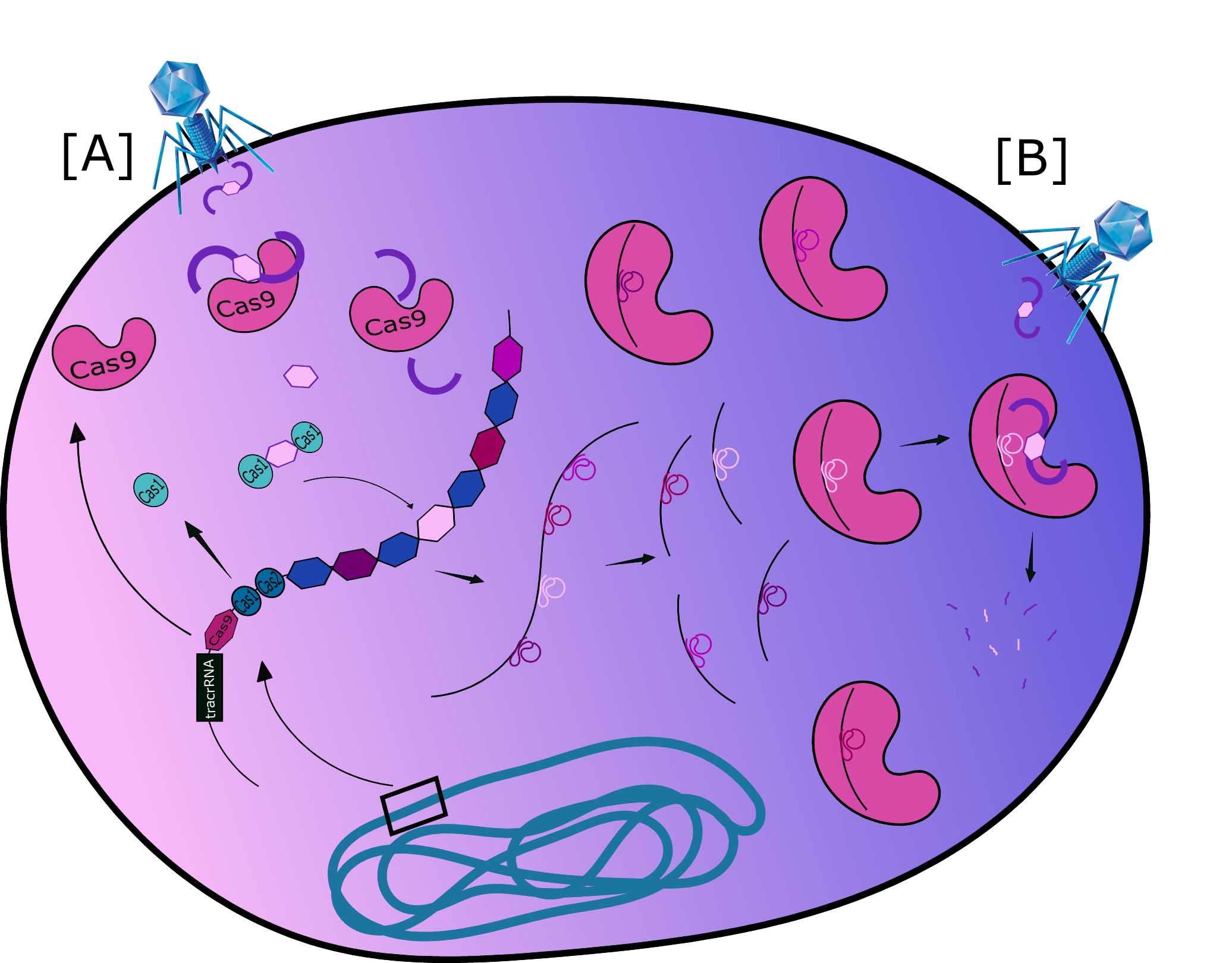 |
| Mecanismo de CRISPR/Cas9 na bactéria mostrando a primeira (A) e a segunda infecção (B). |
O uso deste mecanismo com a finalidade de desenvolver uma cura para AIDS não é uma novidade. Diversos testes têm sido realizados ao longo dos anos, no entanto, nenhum oferecia a esperança de uma melhora completa ao paciente. Uma das mais eficientes tecnologias desenvolvidas em laboratório, a qual impedia o ingresso do vírus no corpo, ao ser aplicada em humanos, poderia comprometer a saúde dos pacientes ao inibir moléculas importantes do sistema imune, expondo-os a outras infecções bacterianas ou virais. Isto porque, como muitas outras metodologias, ela estava focada em suprimir a molécula CD4 dos linfócitos T, que reconhece o HIV e permite que este ingresse na célula humana.
|
|
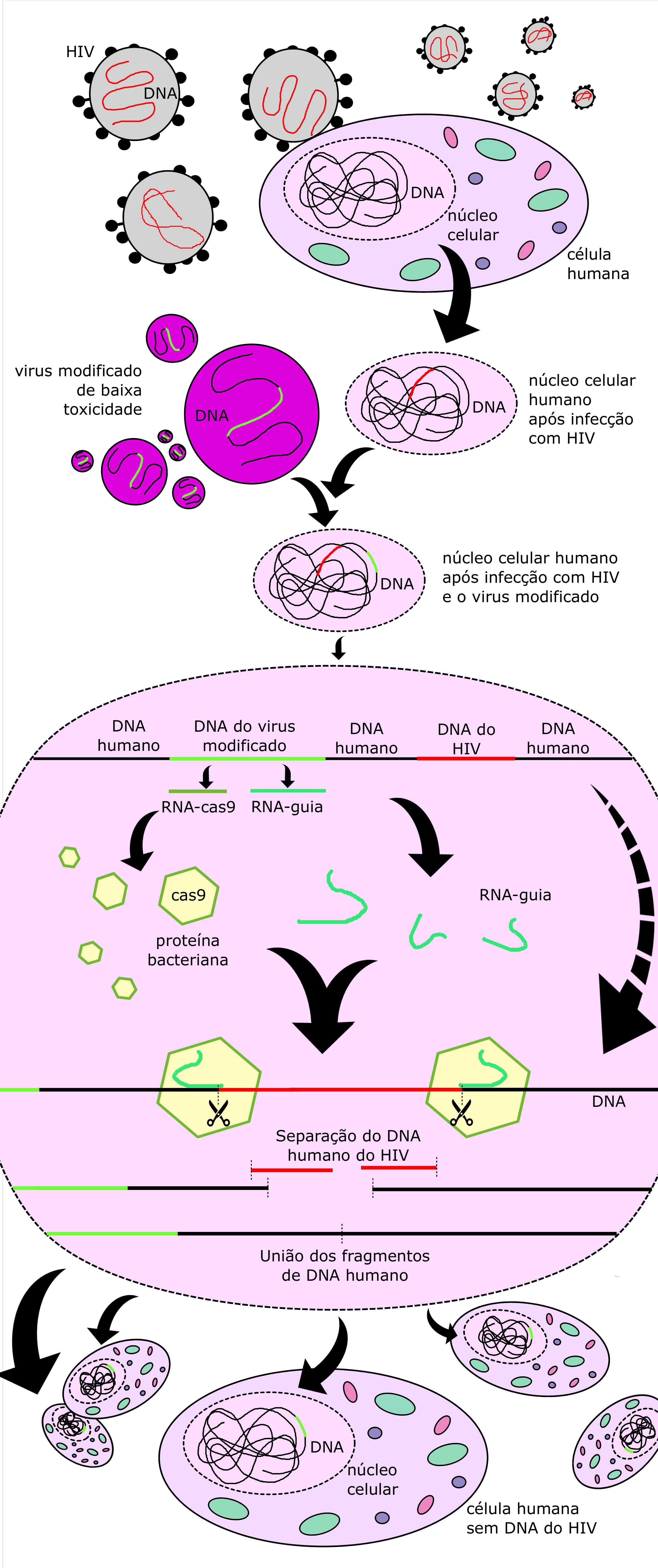
| Mecanismo de eliminação do DNA viral da célula humana mediante uso do sistema CRISPR/Cas9. |
O sistema CRISPR/Cas9 é altamente específico e apresenta a grande vantagem de ser programável, ou seja, é possível programar a Cas9 para eliminar qualquer parte indesejada do DNA de uma célula humana. Para a eliminação do HIV de linfócitos T humanos, pesquisadores sequenciaram o DNA dos linfócitos infectados com o objetivo de identificar o local exato em que o DNA do vírus havia se inserido. Uma vez identificado, modificações na molécula de RNA que se associa à endonuclease Cas9 bacteriana foram feitas de modo que ela passasse a reconhecer regiões do DNA humano próximas ao DNA viral. Para inserir a Cas9 juntamente com o RNA guia nos linfócitos humanos, utilizou-se como vetor um vírus de baixa toxicidade ao qual foram adicionadas tais informações em forma de DNA.
Ao expor o linfócito infectado com HIV a este novo vírus, a célula é infectada da mesma forma e o DNA viral é inserido no DNA humano, forçando a própria célula a expressar a molécula de RNA guia e a Cas9. Uma vez expressas ambas as moléculas, elas se encarregam de cortar especificamente o DNA nos pontos de união, separando o DNA humano do DNA viral. Posteriormente, os dois trechos separados do DNA humano se unem novamente por meio do sistema de reparo celular. Ainda que testes em outros tipos celulares devam ser realizados para validar a eficiência do tratamento com CRISPR/Cas9, a ausência de erros no corte e manipulação do DNA, somado com a não evidência de morte celular nos dá uma esperança de que a Ciência avança e se aproxima cada vez mais da cura definitiva da AIDS.
É evidente que ainda há um longo caminho a ser percorrido na busca por um tratamento disponível 100% efetivo contra a AIDS. A letalidade do vírus tem revelado a vulnerabilidade da espécie humana, dado que a epidemia já matou 39 milhões das 78 milhões de pessoas infectadas desde que se tiveram casos registrados a partir de 1980 (relatório da ONU, 2014). Nesse contexto, é fascinante que a possível cura possa vir do uso dos primitivos mecanismos de defesa das bactérias. Os avanços na ciência nos surpreendem novamente ante a ideia de poder editar nosso próprio DNA para incorporar informação bacteriana que permita destruir o DNA viral, mostrando que, ainda que vulneráveis, somos capazes de criar nossas próprias defesas observando outras espécies.
Leituras sugeridas
- Huang Z, Tomitaka A, Raymond A, Nair M. Current application of CRISPR/Cas9 gene-editing technique to eradication of HIV/AIDS. Gene Therapy, doi: 10.1038/gt.2017.35 (2017).
- Kaminski R, Chen Y, Fischer T, Tedaldi E, Napoli A, Zhang Y, Karn J, Hu W, Khalili K. Elimination of HIV-1 Genomes from Human T-lymphoid Cells by CRISPR/Cas9 Gene Editing. Scientific Reports 6, doi: 10.1038/srep22555 (2016).
- Sander JD, Joung JK. CRISPR-Cas systems for editing, regulating and targeting genomes. Nature Biotechnology 32, 347-355, doi: 10.1038/nbt.2842 (2014).
- Marraffini LA, Sontheimer EJ. CRISPR interference: RNA-directed adaptive immunity in bacteria and archaea. Nature Reviews Genetics 11, 181-190, doi:10.1038/nrg2749 (2010).
- UNAIDS Brasil [Internet]. Estatísticas: Relatórios mais recentes do UNAIDS. Acesso em 8 de novembro de 2017. Disponível em: http://unaids.org.br/estatisticas/